
学术园地
韩雅玲 院士 沈阳军区总医院心血管内科,沈阳 110016
本文刊登在《中国实用内科杂志》,2015,35(1):3-7
关键词:阿司匹林抵抗;冠心病 Keywords:aspirin resistance;coronary heart disease
抗血小板药物是防治心血管疾病、预防血栓事件的重要手段。但是不同个体对于抗血小板药物治疗反应存在差异, 这一现象被称为血小板反应多样性。随着药物的广泛应用, 人们发现, 部分接受抗血小板药物治疗的患者仍然发生血栓事件, 被称为“抗血小板药物抵抗”。阿司匹林作为经典的抗血小板药物, 是冠心病二级预防的基石, 多项研究证实了阿司匹林在冠心病二级预防的显著疗效。然而同其他抗血小板药物一样, 阿司匹林同样存在抵抗现象。
1994 年, “阿司匹林抵抗”这一术语首次使用。近年来随着介入治疗及新型抗血小板药物研究的不断发展, 阿司匹林抵抗问题越来越引起临床的重视。本文将针对阿司匹林抵抗的定义、相关机制、实验室检测、临床影响及可能有效的治疗干预措施等相关新进展简单概述。
1、阿司匹林抵抗的定义
近 5 年, 出现了阿司匹林反应多样性的概念, 主要是基于特定的病理生理机制和药物的药物代谢动力学 (pharmacokinetics, PK) 和(或) 药效动力学 (pharmacodynamics, PD) 产生的。而阿司匹林抵抗只是导致个体对阿司匹林反应多样性的一个可能原因。欧洲心脏病协会血栓工作组 2009 年发布了口服抗血小板药物反应多样性共识, 亦将阿司匹林抵抗分为两类, 即临床抵抗和实验室抵抗。临床抵抗指患者在服用阿司匹林时发生心血管事件; 实验室抵抗指在使用阿司匹林的情况下体外血小板活性仍未被充分抑制。
2、阿司匹林抵抗发生的可能机制
目前已有多项研究对阿司匹林抵抗的发生机制进行了探究。多种原因可影响阿司匹林抑制血栓素 A2(thromboxane A2, TXA2)的产生和激活以及抑制血小板聚集, 从而引起实验室阿司匹林抵抗;亦有多方面因素可导致阿司匹林治疗失败(临床阿司匹林抵抗), 导致临床动脉粥样硬化血管事件发生(图1)。
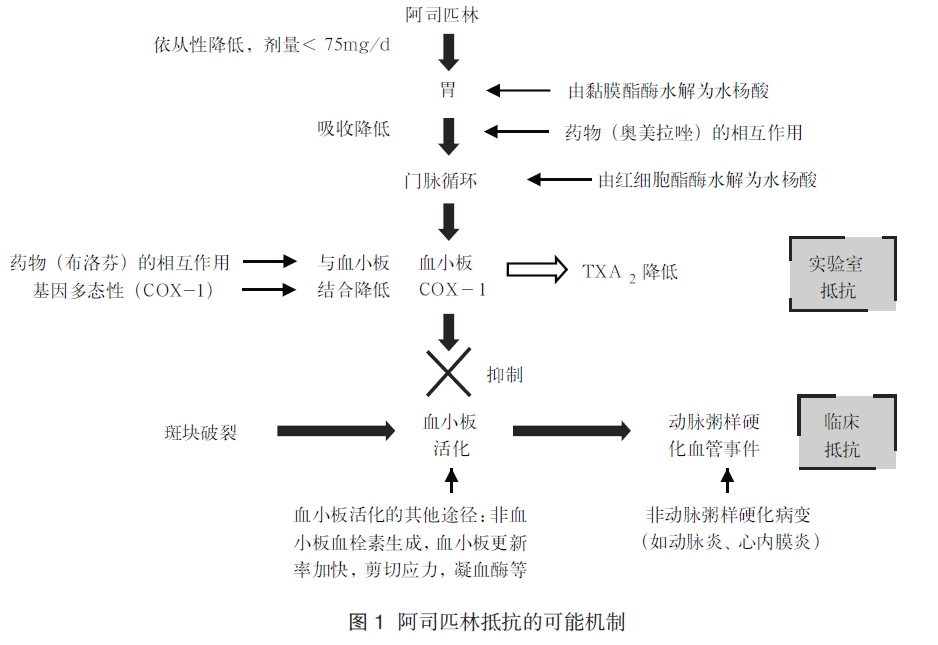
2.1 依从性
多项研究数据显示, 高达 40% 的心血管病患者阿司匹林依从性差。依从性差是阿司匹林实验室或临床作用无效的一个常见的、且易被忽视的原因。Cuisset 等的一项研究显示, 在 136 例行冠脉支架置入的患者中, 出院 1 个月后有 19 例 (14%) 患者被认定为对阿司匹林治疗无反应, 但在经过阿司匹林确认给药后,除 1 例患者外, 所有无反应者均变为有反应, 因此认定这些患者仅是阿司匹林不依从, 而非真正存在生物学上的阿司匹林抵抗。
2.2 剂量
尽管实验室研究表明低剂量阿司匹林也可有效抑制血小板环氧化酶 (cyclooxygenase, COX)-1。但阿司匹林剂量过低与阿司匹林抵抗的发生仍可能存在一定的关联。抗栓协作组 2002 年的荟萃分析显示, 阿司匹林剂量低于 75 mg/d 的疗效是不确定的。 2005 年发表在 American Journal of Medicine 的一项研究发现共 128 例 (27.4%) 患者发生阿司匹林抵抗, 其阿司匹林服用平均剂量显著低于未发生阿司匹林抵抗的患者[(101.95±17.84) mg 对 (114.40±42.17) mg, P<0.001]; 多因素分析显示, 阿司匹林剂量 <100 mg 是阿司匹林抵抗的独立预测因素 (OR 2.23, 95%CI 1.12~4.44,P=0.022)。
2.3 药物间的相互作用
阿司匹林与其他药物如非甾体抗炎药 (NSAIDs) 或 COX-2 抑制剂联用时, 可能会由于药物间的相互作用, 导致阿司匹林药代动力学抵抗的发生。如布洛芬可拮抗阿司匹林引起的血小板不可逆抑制作用。萘普生亦可干扰阿司匹林对血小板 COX-1 活性和功能的抑制作用。此外, 他汀类药物亦能影响阿司匹林抵抗的发生, 研究显示在使用他汀的患者中阿司匹林抵抗的发生率更高。 Feher 等进行的一项研究显示, 即使在经过危险因素和药物使用校正后, 使用他汀类药物仍然是阿司匹林抵抗的独立预测因子 (OR 5.92, 95%CI 1.83~16.9, P<0.001)。
2.4 基因多态性
基因因素可能在阿司匹林抵抗中具有重要作用。一项针对 124 例急性心肌梗死患者的研究发现, COX1-A1 基因变异与阿司匹林抵抗发生显著相关; 一项针对 450 例接受阿司匹林治疗的中国老年人群的研究显示: 糖蛋白Ⅲa 基因 (GPⅢa) 基因多态性与中国老年人群出现阿司匹林抵抗相关。
2.5 血小板更新率加快
冠状动脉搭桥术、感染及炎症期间血小板更新率加快, 可引起 24 h 给药间隔期内未被阿司匹林抑制的血小板比例增加(阿司匹林的半衰期很短), 表现为血小板 COX-1 抑制不足。
2.6 其他可能原因
最近的一项研究显示, 阿司匹林抵抗患者血小板糖蛋白Ⅲa 受体的表达显著增加, 但在阿司匹林敏感患者中不会出现这一现象, 这一发现为阿司匹林抵抗机制的探索提供了新的线索, 且血小板糖蛋白Ⅲa 受体可能作为一种新的生物标志物用以确定阿司匹林抵抗的发生。
还有研究称阿司匹林抵抗与年龄相关, ≥ 75 岁的冠心病患者阿司匹林抵抗发生率高。有研究称阿司匹林肠溶剂型可能引起阿司匹林抵抗, 低剂量肠溶阿司匹林作为心血管病二级预防用药可能因生物利用度不充分而无法达到完全抑制血小板 COX, 而药物学家则认为此现象是因肠溶包衣导致药物吸收延迟和减少而出现的“假抵抗”现象。吸烟患者可能会由于香烟的促凝血作用导致阿司匹林抵抗。其他因素如非血小板血栓素生成、非动脉粥样硬化病变等均可能与阿司匹林抵抗发生有一定的联系。
3、阿司匹林抵抗对冠心病患者临床预后的影响
对于使用阿司匹林作为二级预防的冠心病患者, 若发生阿司匹林抵抗, 可能会增加患者的心血管病风险。
对于稳定性心血管病患者, 研究证实阿司匹林抵抗与患者主要不良事件风险超过 3 倍相关。一项纳入 326 例使用阿司匹林(325 mg/d, ≥ 7 d) 的稳定性心血管病患者的临床研究, 旨在探讨阿司匹林抵抗与长期临床事件的关系, 平均随访 (679±185)d, 结果显示, 与阿司匹林敏感者相比, 阿司匹林抵抗显著增加死亡、心肌梗死或脑血管意外风险 (HR 3.12, 95%CI 1.10~8.90, P=0.03)。
Pamukcu 等研究探究急性冠状动脉综合征 (acute coronarysyndromes, ACS) 患者阿司匹林抵抗的发生率及随访期间阿司匹林抵抗对临床预后的影响。血小板功能分析 (platelet functionanalyzer, PFA)-100 测定显示19% 的患者存在阿司匹林抵抗。随访期间, 阿司匹林抵抗组 45% 的患者发生主要心血管不良事件 (MACE), 阿司匹林敏感组仅 11.7% 的患者发生 MACE (P=0.001)。多因素分析显示阿司匹林抵抗是 ACS 患者主要MACE 发生的独立预测因子。
荟萃分析同样证实阿司匹林抵抗与心血管病患者的临床预后具有显著相关性。 Krasopoulos 等进行的一项荟萃分析中 2120 例患者确定为对阿司匹林敏感, 810 例患者存在阿司匹林抵抗。结果显示, 阿司匹林抵抗患者心血管事件发生率明显高于阿司匹林敏感患者 (39% 对 16%, OR 3.86,95%CI 3.08~4.80, P<0.001)。此外, 阿司匹林抵抗患者死亡风险亦显著增加 (OR 5.99, 95%CI 2.28~15.72, P<0.003)。结果提示, 与阿司匹林敏感者相比, 阿司匹林抵抗患者非致命和致命性心血管、脑血管或血管事件风险增加约 4 倍, 且这一风险增加情况在各种存在心血管或脑血管事件的群体中具有普遍性。
2014 年发表的一篇荟萃分析结果显示, 1889 例冠心病患者中有 622 例确定为阿司匹林抵抗, 阿司匹林抵抗患者不良事件风险显著高于阿司匹林敏感患者(OR 2.44,95%CI 1.81~3.30,P<0.01)。即对于接受阿司匹林治疗依从性好的冠心病患者, 阿司匹林抵抗可使患者 MACE 风险增高约 2.4 倍。
4、阿司匹林抵抗的实验室检测方法
4.1 光学凝集
利用分光光度计 (TLA) 测量血小板聚集时的透光度改变。此方法能较好地反映临床结果, 被认为是测定血小板聚集功能的“金标准”, 同时也是抗血小板药治疗及阿司匹林抵抗最常用的实验室监测指标之一, 但其特异性不高, 对样本含量以及操作的技术要求较高, 容易出现误差。
4.2 VerifyNow
测试原则与光学凝集法相同, 是一个简单的床边测试方法, 测量血小板对纤维蛋白原和花生四烯酸的凝集反应。其优点是需血量少, 操作简单、迅速, 能够完成床旁检测。用于阿司匹林抵抗检测敏感性以及特异性较好, 是目前比较推崇的方法, 但是费用较昂贵。
4.3 PFA-100(血小板功能分析仪)
PFA-100 测量由高血液流速和血小板活化剂如胶原肾上腺素引起的血小板聚集。该测试系统自动且快速。目前认为, 此方法是诊断血小板异常性疾病的理想工具之一, 也是检测阿司匹林抵抗最可信、最有效的指标。其对标本要求较严格, 采血后须 4~6 h 内完成检测。
4.4 出血时间
该方法是通过皮肤穿刺测量出血时间, 该方法是最早也是惟一在体内进行的血小板功能检测方法, 简单、易于操作且不需要血液制备过程, 但并不常用。因此, 由于各种检测方法均存在各种缺陷, 目前主要用于实验研究, 尚无法在临床广泛开展。
5、阿司匹林抵抗的治疗措施
目前有研究证实, 针对导致阿司匹林抵抗发生的可能机制所采取的一系列措施, 如增加阿司匹林剂量、改善患者依从性、增加使用频率、增加新药等。可改善患者对阿司匹林治疗的反应性, 从而降低阿司匹林抵抗的发生。
5.1 增加阿司匹林剂量
由于个体间对阿司匹林治疗反应存在差异性, 因此, 不同患者可能需要不同剂量阿司匹林治疗以达到理想的血小板抑制作用。增加阿司匹林剂量可能改善阿司匹林抵抗。
一项研究旨在探究对于存在阿司匹林抵抗的不稳定性心绞痛或非 ST 段抬高心肌梗死患者, 阿司匹林剂量由 150 mg/d 增加至 300 mg/d 是否可达到更好的治疗效果, 结果显示, 服用 150 mg/d 的患者与服用 300 mg/d 患者比较, 两组间患者二磷酸腺苷(ADP)诱导的血小板聚集率、胶原诱导的血小板聚集比例及血栓素 B2 (TXB2) 的差异具有统计学意义 [分别为 (66±7.01)%、 (62±4.34)%、 (620±64.58) ng/L 对 (26.87±2.85)%、 (16.5±3.8)%、 (77±11.3) ng/L], 提示增加阿司匹林剂量可改善阿司匹林抵抗。
另一项纳入 485 例稳定性冠状动脉疾病患者的研究同样证实提高阿司匹林剂量可改善阿司匹林抵抗。 2013 年的一项研究纳入 40 例冠心病患者, 经 Verify Now 法检测, 这些患者已对阿司匹林 75 mg/d 产生抵抗, 加服至 150 mg/d 4 周后重复检测, 发现 62.5% 的患者成功克服阿司匹林抵抗。
需要注意的是, 随着新型强效 P2Y12 受体拮抗剂的使用, PLATO 等研究的数据分析表明, 增加阿司匹林剂量并不能改善临床事件, 反而增加出血风险。因此, 在与 P2Y12 抑制剂合用时, 即使血小板功能检测结果提示阿司匹林治疗反应不佳, 也不推荐增加阿司匹林剂量, 近期指南推荐对于行经皮冠状动脉介入治疗 (PCI) 患者在使用阿司匹林联合 P2Y12 抑制剂进行双联抗血小板治疗时, 阿司匹林的使用剂量应由刚开始的负荷剂量 150~300 mg 减至 75~100 mg/d, 可见目前增加剂量改善阿司匹林抵抗的研究大多仅针对于阿司匹林单一抗血小板治疗或停用双联抗血小板治疗后的患者, 而可能不适用于阿司匹林与 P2Y12 受体拮抗剂合用的情况。
5.2 改善用药依从性
通过提高患者对阿司匹林的依从性同样可降低阿司匹林抵抗发生率。一项观察性研究共纳入 212 例具有心肌梗死病史的患者, 患者起始接受阿司匹林 100 mg 治疗, 通过 PFA-100 血小板功能分析结果显示, 33 例 (18.4%) 发生阿司匹林抵抗, 对 33 例阿司匹林抵抗患者用药依从性进行更严格的控制, 1 周后结果显示, 33 例患者中有 11 例不再出现阿司匹林抵抗。最后, 将 22 例仍存在阿司匹林抵抗患者的用药剂量增加至 200~300 mg/d, 治疗 4 周后, 检测结果显示仅 3 例 (1.4%) 存在阿司匹林抵抗。该研究结果提示, 对于存在阿司匹林抵抗的急性心肌梗死的患者, 加强依从性和增加阿司匹林剂量 (从 100 mg 增至 200~300 mg) 可使阿司匹林抵抗发生率从 18.4% 降至 1.4%。
5.3 增加阿司匹林使用频率
研究证实增加阿司匹林使用频率也是降低阿司匹林抵抗发生率的一种有效手段。一项共纳入 92 例患者的单中心交叉试验结果显示, 在糖尿病合并冠状动脉疾病患者中, 阿司匹林每日 2 次给药方案阻断血小板聚集的效果明显优于总剂量相同的每日 1 次给药方案。研究开始时, 受试者被随机分配至阿司匹林 150 mg 组(每日清晨服用) 或者阿司匹林 75 mg 组(清晨和晚上各服用 1 次), 连续服用 7~14 d 后抽取血样。采血后, 受试者立即交换给药方案, 再连续服用 7~14 d, 然后进行第二次采血。
研究者采用 TLA 法检测了每份血样的血小板聚集情况以评估阿司匹林抵抗, 最大聚集率≥ 20% 的血样被视为存在阿司匹林抵抗。检测结果显示, 阿司匹林每日 1 次给药时有 39 例患者(42%)出现了阿司匹林抵抗, 而每日 2 次给药时只有 16 例患者 (17%) 出现了阿司匹林抵抗, 差异有统计学意义 (P=0.0004)。交换给药方案后, 39 例在接受每日 1 次给药期间出现阿司匹林抵抗的受试者改为每日 2 次后, 有 24 例 (62%) 对阿司匹林产生了应答。
相反, 16例在每日 2 次给药期间出现阿司匹林抵抗的受试者改为每日 1 次后, 只有 1 例 (6%) 产生应答。针对可能影响阿司匹林抗血小板效应的因素开展的多变量分析表明, 与每日 1 次治疗相比, 每日 2 次治疗与阿司匹林抵抗发生率下降 79% 相关, 差异有统计学意义 (RR 0.21, 95%CI 0.09~0.46, P<0.001)。
5.4 增加其他抗血小板药物
近期研究表明加用氯吡格雷的双联抗血小板治疗也是一种治疗阿司匹林抵抗的可行方法。一项研究纳入行非体外循环冠状动脉旁路移植术的 60 例患者, 随机分为两组, 分别予阿司匹林 100 mg/d 进行单抗治疗或阿司匹林 100 mg加氯吡格雷 75 mg/d 进行双联抗血小板治疗。用药后第 1、2 天进行血小板聚集功能检测发现, 双联抗血小板治疗较单抗治疗阿司匹林抵抗的发生率更低 (32.1% 对 62.1%, 10.7% 对 34.5%, P<0.05)。
5.5 其他措施
其他降低阿司匹林抵抗发生率的措施, 如避免药物间相互作用、治疗并发症及选择合适剂型等, 有待进一步的临床研究以证实其疗效。
6、小结
阿司匹林抵抗是一种可以导致治疗失败的临床现象, 对冠心病患者的临床预后有显著的影响。由于缺乏合适的实验室诊断方法以及阿司匹林抵抗发生的确切机制尚未明确, 目前对于阿司匹林抵抗的诊断和治疗措施均存在一定的局限性和争议, 今后我们需要更多的研究来支持如何恰当地界定和管理阿司匹林抵抗。






